ACE2発現iPS+CRISPRiで、感染関連受容体とプロテアーゼの機能を比較
京都大学iPS細胞研究所(CiRA)は10月21日、新型コロナウイルス(SARS-CoV-2)感染においてTMPRSS2とカテプシンBが重要な役割を担うことを見出したと発表した。この研究は、CiRA増殖分化機構研究部門の橋本里菜特定研究員、高山和雄講師らの研究グループによるもの。研究成果は、「Molecular Therapy-Nucleic Acids」にオンライン公開されている。
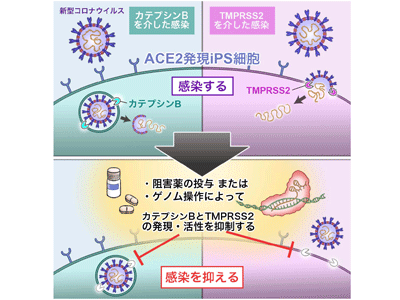
画像はリリースより
新型コロナウイルス感染症(COVID-19)の治療薬を開発するためには、SARS-CoV-2の感染メカニズムを十分に解明する必要がある。SARS-CoV-2のスパイク(S)タンパク質は、細胞表面に発現するACE2に結合したのち、TMPRSS2等のプロテアーゼによって切断される。切断されたSタンパク質は細胞膜とウイルス外膜を融合させることにより、SARS-CoV-2の細胞内への侵入を促進する。そのため、SARS-CoV-2はACE2とTMPRSS2発現に依存して、感染すると考えられている。ところが最近、ACE2とTMPRSS2以外にも、複数の受容体やプロテアーゼがウイルス感染に重要な役割を担うことが相次いで報告されている。しかし、これらの受容体やプロテアーゼの機能を比較した報告はほとんどない。
今回、研究グループは、SARS-CoV-2感染に関わる受容体とプロテアーゼの機能を比較するために、iPS細胞およびCRISPRi技術を用いた。iPS細胞においてCRISPRi技術を用いることで、標的の遺伝子の発現を約1%以下にまで抑制できることが報告されている。さらに、iPS細胞はあらゆる体細胞に分化できるため、標的の遺伝子を発現抑制した体細胞を作製することも可能だ。
研究グループは、未分化iPS細胞にSARS-CoV-2が感染するためにはACE2が不可欠であることを最近報告しており、ACE2発現iPS細胞を作製することで、ウイルスが感染・複製できることを確認している。今回、ACE2発現iPS細胞およびCRISPRi技術を用いて、SARS-CoV-2感染に関わる受容体とプロテアーゼの機能を比較した。
カテプシンB、カテプシンL、TMPRSS2遺伝子抑制で感染低下
まず、ACE2以外で、これまでにSARS-CoV-2感染への関与が報告されている3種の受容体(NRP1、BSG、IFNAR2)と6種のプロテアーゼ(TMPRSS2、TMPRSS4、TMPRSS11E、TMPRSS13、カテプシンB、カテプシンL)の機能を比較検証した。
CRISPRi技術を用いてiPS細胞の標的遺伝子の発現量を低下させたのち、ACE2を過剰発現させた上で、SARS-CoV-2感染実験を実施。その結果、評価した受容体とプロテアーゼのうち、カテプシンB、カテプシンL、TMPRSS2については、遺伝子の発現量を低下させることにより、ACE2発現iPS細胞におけるウイルスRNAコピー数はそれぞれ11.7%、0.84%、20.6%に低下した。したがって、検討した受容体とプロテアーゼのうち、カテプシンB、カテプシンL、TMPRSS2遺伝子は、iPS細胞におけるSARS-CoV-2感染に関与することが示唆された。
女性細胞はカテプシンB阻害剤、男性細胞はTMPRSS2阻害剤で感染阻害可能
次に、ACE2発現iPS細胞を用いて、カテプシンB、カテプシンL、TMPRSS2の阻害剤がSARS-CoV-2感染を阻害可能か調べた。TMPRSS2遺伝子発現量には性差があるため、男女由来の2種類のiPS細胞にそれぞれACE2を発現させた後、SARS-CoV-2を感染させた。そこへ、カテプシンB阻害剤であるCA-074 Me、カテプシンL阻害剤であるZ-Phe-Tyr(tBu)-diazomethylketone、TMPRSS2阻害剤であるカモスタット(Camostat)およびナファモスタット(Nafamostat)を作用させた。
その結果、女性由来のACE2発現iPS細胞において、CA-074 Meを作用させることによりウイルスRNAコピー数が0.62%にまで減少しました。一方で、男性由来のACE2発現iPS細胞においては、カモスタットおよびナファモスタットを作用させることによりウイルスRNAコピー数がそれぞれ0.48%、0.23%にまで減少した。阻害剤作用後の細胞生存率を調べると、ナファモスタットを作用した細胞では極端に生存率が低く、ナファモスタットには強い細胞毒性があることわかった。以上のことから、CA-074 Meとカモスタットが、ACE2発現iPS細胞におけるSARS-CoV-2の感染を阻害できることが示唆された。
カテプシンB阻害+TMPRSS2阻害で男女とも感染阻害、細胞毒性ほぼなし
最後に、カテプシンBとTMPRSS2の両方を阻害することにより、感染阻害効率が向上するかを調べた。まず、CRISPRi技術を用いてiPS細胞のカテプシンBおよびTMPRSS2両遺伝子の発現量を低下させたのち、SARS-CoV-2を感染させた。その結果、ウイルスRNAコピー数は0.036%にまで低下した。
阻害剤による効果を確認するため、男女合わせて6種類のサンプルにおいてCA-074 Meとカモスタット(CA-074 Me+CAM)による作用を調べた。その結果、CA-074 Meとカモスタットを組み合せることで、ウイルスRNAコピー数が約0.0078%にまで低下することを確認。このとき、2種類の阻害剤の組み合せによる細胞毒性はほとんど見られなかった。また、2種類の阻害剤の組み合せにより、SARS-CoV-2感染による細胞死の回避とSARS-CoV-2ヌクレオカプシドタンパク質陽性細胞の減少も観察された。
なお、今回の研究で用いた新型コロナウイルスはB.1.3株だったが、他の3種類のSARS-CoV-2変異株(B.1.1.7、B.1.351、 B.1.1.248)においても同様の効果が観察された。以上のことから、CA-074 Meとカモスタットが相乗的にウイルス感染を阻害できることが示唆された。
完全な感染阻害に向けた今後の研究に今回の技術は有用
今回の結果から、SARS-CoV-2がACE2発現iPS細胞に感染するためには、カテプシンBとTMPRSS2が必要であることが明らかになった。TMPRSS2は細胞膜に存在し、カテプシンBはエンドソームに存在している。したがって、エンドサイトーシス経路を通らないケースではTMPRSS2が、エンドサイトーシス経路ではカテプシンBが重要な役割を担うことが示唆された。
今回の研究では、CA-074 Meとカモスタットの組み合せにより、ウイルス感染効率の顕著な低下が見られたが、完全な感染阻害効果を得ることはできなかった。今回調べた受容体とプロテアーゼ以外にも重要な因子があると予想される。今回用いたACE2発現iPS細胞およびCRISPRi技術は、新たなSARS-CoV-2関連因子の探索と評価にも使用できると考えられる。さらに、sgRNA発現ライブラリーを用いることで、ウイルス感染に必須の新たな因子の同定が期待される。
今回はACE2発現iPS細胞におけるSARS-CoV-2受容体とプロテアーゼの機能解明を行ったが、肺胞上皮細胞や気道上皮細胞、心筋細胞、腸管上皮細胞などの体細胞でも同様に検証する必要がある。受容体とプロテアーゼの発現プロファイルは体細胞ごとに異なるため、各体細胞におけるこれらの遺伝子の寄与度は異なると予想される。今後、同研究グループが樹立したACE2発現iPS細胞を各体細胞へ分化させることで、各体細胞における受容体とプロテアーゼの解析も期待できる。
▼関連リンク
・京都大学iPS細胞研究所(CiRA)ニュース








