「ヒット&ラン」型発がんモデルの真偽を検証
東京大学は5月17日、ピロリ菌 CagAがゲノム安定性を司るBRCA1の機能を障害することで、胃上皮細胞のがん化に必要な遺伝子変異の蓄積を誘発することを明らかにしたと発表した。この研究は、同大大学院医学系研究科の畠山昌則教授、紙谷尚子講師らのグループと、同研究科石川俊平教授、牛久哲男教授らとの共同研究によるもの。研究成果は、「Cell Host & Microbe」電子版に掲載されている。
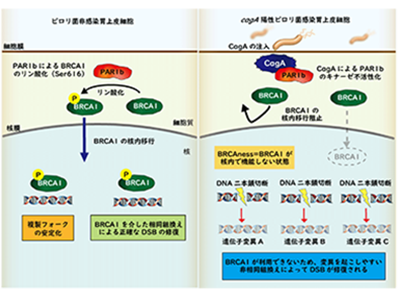
画像はリリースより
ヘリコバクター・ピロリ(ピロリ菌)CagAタンパク質は、細菌の注射針様装置により胃上皮細胞内に注入される。ピロリ菌が感染した細胞(宿主細胞)内に侵入したCagAは発がん性ホスファターゼSHP2と結合しその活性を脱制御する一方、極性制御キナーゼPAR1bとも結合し、その活性を不活化する。CagAによるこれら宿主細胞内標的分子の機能撹乱が胃がん発症に重要な役割を果たすと考えられてきたが、ひとたび生み出された胃がん細胞のがん形質維持にCagAはもはや不要であり、胃発がんのプロセスにおいてCagA依存的ながん前駆細胞がCagA非依存性を獲得する機序が大きな謎として残されてきた。
そうした中、ピロリ菌CagA自身が宿主細胞のゲノム不安定化(遺伝子変異の異常な蓄積)を誘導し、細胞がん化に関わるCagAの役割が複数の宿主遺伝子変異によって取って代わられた結果、CagA非依存的ながん細胞が生み出されるという「ヒット&ラン」型発がんモデルが提唱された。研究グループは今回、この発がんモデルを検証するため解析を行った。
ピロリ菌 CagAがBRCA1の機能を障害し、胃がん発症につながる遺伝子変異蓄積を誘発
胃上皮細胞内に侵入したピロリ菌CagAが宿主細胞ゲノムに傷害を与えるか否かを解析した結果、CagAはPAR1bのキナーゼ(タンパク質リン酸化酵素)活性の不活化を介して、宿主ゲノムに重篤なDNA損傷であるDNA二本鎖切断(DSB)を誘発することが明らかとなった。
DSBは核内の現象であるのに対し、CagA-PAR1b複合体は細胞膜近傍に形成されるため、DSB制御に関わる分子群の中で細胞質と核の間をシャトル(行き来)する分子に着目して解析を進めた結果、CagAによるPAR1bのキナーゼ抑制がBRCA1の核内移行を著しく抑制することを見出した。さらにその分子機序を検討したところ、BRCA1の細胞質-核移行にはBRCA1の核移行シグナル近傍に存在するセリン残基(Ser616)のPAR1bによるリン酸化が必須であることが判明。核内BRCA1の減少・枯渇は「DSBにつながる複製フォークの不安定化」ならびに「相同組換え依存性修復機能の欠損」で特徴づけられる異常な細胞状態(BRCAness)を引き起こし、遺伝子変異蓄積の場となるゲノム不安定化が誘導されることが示された。一般に、DSBのような重篤なゲノム損傷が蓄積すると細胞死が引き起こされるが、CagA発現細胞では細胞死は認められなかった。この細胞死回避機構を追究したところ、CagAはPAR1bのキナーゼ活性阻害を介してBRCAnessを誘導すると同時にHippoシグナルを活性化することでDSB特異的な細胞死を阻止し、ゲノム変異が蓄積した細胞(がん前駆細胞)の生存を可能にしていることが明らかになった。
「ヒット&ラン」型発がんモデルの分子基盤を実証
同研究の妥当性を臨床的に検証するため、手術材料から得られた胃粘膜組織におけるBRCA1の発現・細胞内分布を解析したところ、cagA陽性ピロリ菌が数多く存在する胃粘膜表面を構成する上皮細胞(表層粘液細胞)では核内BRCA1がほぼ消失しており、胃底腺内部においても幹細胞ならびに増殖細胞が存在する狭部においてピロリ菌近傍に位置する上皮細胞で核内BRCA1の著しい減少とDSBの形成が認められた。
以上の結果から、CagA-PAR1b相互作用が「BRCAnessの誘導」と「ゲノム損傷細胞の死の回避」を同時に引き起こすことで、CagA非依存的ながん細胞の生成につながる異常な宿主細胞ゲノム変異の蓄積が生みだされることが明らかとなり、胃がん発症のプロセスが、胃上皮細胞へのピロリ菌CagAの「奇襲と逃亡」の繰り返しを介して進行するという「ヒット&ラン」型発がんモデルの分子基盤が実証された。
PARP阻害剤・DNA複製阻害剤とHippoシグナル不活化剤の併用が胃がん治療に応用できる可能性
今回の研究により、胃上皮細胞に侵入したピロリ菌CagAががん化につながる遺伝子変異を宿主細胞ゲノムに積極的に蓄積させるメカニズムが解明された。同研究成果は、胃がんが乳がんや卵巣がんと共通した発がん環境(BRCAness)を経て発症することを意味している。胃がんがBRCAnessおよびHippoシグナルの活性化を介して発症するという事実は、現在BRCAnessを呈するがんに使用されているPARP阻害剤・DNA複製阻害剤とHippoシグナル不活化剤の併用が胃がん治療に応用できる可能性を示している。
「本研究は胃がん予防のための早期ピロリ菌除菌の重要性をより明確に示しており、この成果を基盤とした胃がんならびにBRCA1変異を基盤とする乳がん・卵巣がん・膵臓がんなど、他のがんの革新的な予防法・早期治療法の確立につながることが期待される」と、研究グループは述べている。
▼関連リンク
・東京大学大学院医学系研究科・医学部 プレスリリース








