モデルマウスでの血管の薬剤耐性を確認、ヒトを対象に検討
北海道大学は6月15日、抗がん剤による腫瘍内の炎症性変化が血管に異常性をもたらし、薬剤耐性の原因となることを明らかにしたと発表した。これは同大病院の菊地央医員、樋田泰浩准教授、同大大学院歯学研究院の樋田京子教授、間石奈湖助教、同大学院医学研究院の篠原信雄教授らの研究グループによるもの。研究成果は、「Cancer Research」誌にオンライン掲載されている。
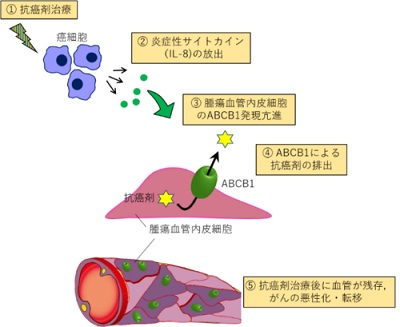
画像はリリースより
がんが局所で進行し手術不能となった場合や転移症例には、多くの場合、抗がん剤治療が行われるが、薬剤への耐性出現は予後不良の大きな要因で、その克服は治療上重要な課題の一つだ。一方、がん組織内の血管は、がんに栄養・酸素を運び、転移の経路にもなるためがんの悪性化に重要な役割を果たしている。
これまで腫瘍内血管の内側を覆う「腫瘍血管内皮細胞」は、遺伝的に安定で薬剤耐性を獲得しないと考えられていた。しかし、研究グループはこれまでに、腫瘍血管内皮細胞がさまざまな異常性をもつことを明らかにしている。マウスの腫瘍モデルにおいて、腫瘍血管内皮細胞は抗がん剤「パクリタキセル」の排出ポンプABCB1の発現レベルが高く、パクリタキセルに対して耐性があることを世界で初めて明らかにした。さらに血管のABCB1阻害により同剤の治療効果が増強することを示している。通常、薬剤耐性のメカニズムとしてがん細胞の異常が広く知られていたが、血管も薬剤耐性に関与することが示唆された。ただし、ヒトではがんの薬剤耐性における血管の関与は不明のままだ。
これらのことから、研究グループは今回、抗がん剤の一次治療が奏功せず、二次治療としてパクリタキセルが用いられることの多いヒト尿路上皮がんを用いて、腫瘍血管内皮細胞におけるABCB1発現の有無と薬剤耐性への関与、さらに薬剤耐性克服にむけて血管のABCB1阻害の有用性を検討した。
抗がん剤治療後の尿路上皮がん患者の6割でABCB1発現増加、モデルマウスにパクリタキセルとABCB1阻害剤を併用で腫瘍増殖と肺転移を抑制
抗がん剤治療が行われた尿路上皮がん患者を対象とし、一次治療前後の手術摘出組織標本を用いて免疫染色により腫瘍血管におけるABCB1発現を評価し、予後との関連を解析した。続いて、抗がん剤治療が腫瘍血管におけるABCB1発現に影響を及ぼすメカニズムについて、腫瘍血管内皮細胞や膀胱がん細胞を用いて解析した。さらに、膀胱がん担がんマウスモデルを用いて、一次化学療法としてゲムシタビン/シスプラチンを投与後、二次化学療法として投与するパクリタキセルにABCB1阻害剤を併用し、ABCB1阻害剤併用療法の治療効果を検証した。
その結果、抗がん剤治療後の6割以上の患者で、腫瘍血管内皮細胞のABCB1の発現量が増加していた。さらにこうした症例では、ABCB1の発現が変化しなかった患者に比べて予後が不良だった。一方で、がん細胞のABCB1は、抗がん剤治療前後では発現量に有意な差は認められなかった。また、腫瘍血管内皮細胞のABCB1発現が亢進するメカニズムとして、抗がん剤治療後のがん細胞におけるIL-8の分泌量増加が関与していることが判明。膀胱がん担がんマウスに二次化学療法としてパクリタキセルを投与する際、ABCB1阻害剤を併用すると血管新生が抑制され、腫瘍の増殖と肺転移が抑制された。
がんの薬剤耐性克服に向けた治療戦略として、がん細胞のみならず、異常性を獲得した腫瘍血管内皮細胞を標的にした治療が必要と考えられる。その異常性の一つ、腫瘍血管内皮細胞において発現量が増加したABCB1を標的とする阻害剤の開発や効果的な投与法について今後研究が進むものと推測される。「抗がん剤治療により誘導されたがん細胞由来のIL-8が、腫瘍血管内皮細胞の異常性獲得の一つのメカニズムであり、それを防ぐ戦略展開も期待される」と、研究グループは述べている。
▼関連リンク
・北海道大学 プレスリリース








